近年来,3D打印技术兴起和成熟,在骨科椎间融合器领域的应用也崭露头角。相比传统设计,3D打印椎间融合器有利于骨融合的多孔结构,增强放射成像特性,使融合可视化的开放式设计。目前椎间融合器已成为3D打印技术在骨科植入物制造领域产业化推进速度最快的领域之一。
3D打印融合器行业目前现状分析
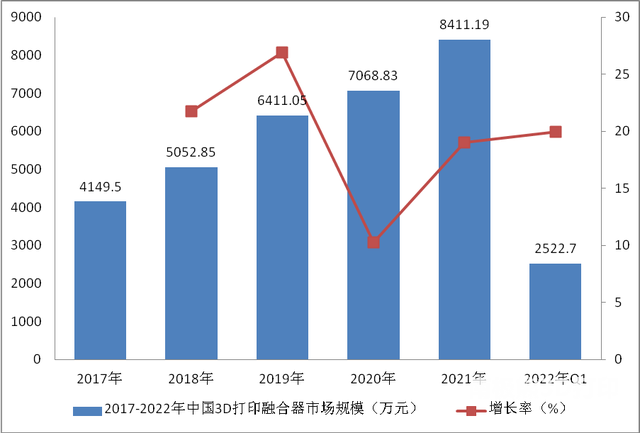
统计数据显示,2017年中国3D打印融合器市场规模4149.50万元,到2021年中国3D打印融合器市场规模8411.19万元,增长率18.99 %。2017-2022年中国3D打印融合器市场规模如下:
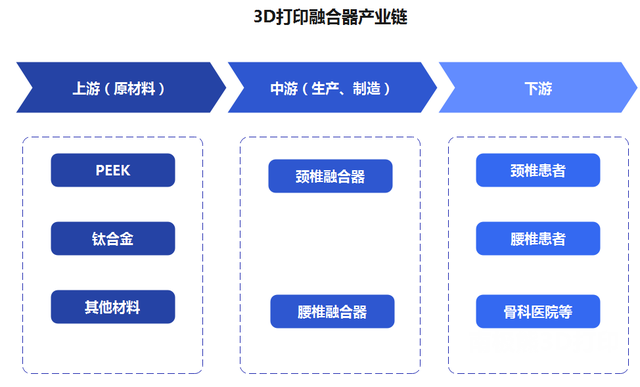
打印融合器产业链分析
3D打印融合器行业发展面临的风险
中国医疗3D打印面临的政策困境
对比国外,中国其实对3D打印技术也非常重视。
2015年2月28日,工信部发布《国家增材制造产业发展推进计划(2015—2016年)》,提出到2016年中国要初步建立较完善的增材制造产业体系,整体技术水平保持与国际同步。
2015年5月19日,国务院印发《中国制造2025》规划,明确将3D打印产业作为发展重点。
2015年9月,中国首个3D打印人体植入物——人工髋关节产品获得国家食品药品监督管理总局注册批准,一时引发了众多关注。
到目前为止,中国有四款产品通过了CFDA认证,分别是:爱康医疗与北医三院合作的3D打印髋臼杯、3D打印人工椎体、3D打印脊柱椎间融合器,以及迈普医学的3D打印硬脑(脊)膜补片。
但是,中国目前在3D打印医疗器械方面仍然监管不足,缺乏相关的审批认证制度方案。

管理制度滞后,累及医疗3D产业健康发展
自2014年《医疗器械监督管理条例》(以下简称《条例》)修订以来,国家发布了众多配套部门规章以及规范性文件,基于医疗器械产品全生命周期初步构建了全程管理体系。该管理体系以医疗器械的质量管理为重心,以医疗器械法规体系和技术标准为两大管理依据。但是,目前针对3D打印医疗器械的管理依据基本处于空白状态。
首先,对于非传统制造工艺生产的3D打印医疗器械,管理部门积累的监管经验极少,对它的生产经营以及使用的管理实践还很欠缺,要在短时间内出台针对性的行政管理规范很难。
其次,严重缺乏相关技术标准。技术标准是医疗器械企业进行研发设计、检验检测、生产经营的重要依据。目前对于采用3D打印技术制备的医疗器械,中国还没有出台任何针对性的国家标准和行业标准。这既给相关企业对3D打印医疗器械的质量控制造成很大的困难,也给监管部门对3D打印医疗器械的技术审评带来很大的障碍。
再次,一些医疗器械质量管理规范如《医疗器械临床试验质量管理规范》(医疗器械GCP)、《医疗器械生产质量管理规范》(医疗器械GMP)、《医疗器械经营质量管理规范》(医疗器械GSP),主要适用于采用传统制造工艺生产的医疗器械,缺乏对3D打印医疗器械质量管理的指引内容。
技术评价受限,影响上市审批进展
目前,对3D打印医疗器械进行技术评价,不论是企业还是监管部门都存在不少的困难。
第一,对3D打印医疗器械进行管理,首先要解决的问题是它的分类。3D打印医疗器械的结构特征和使用形式有别于传统工艺生产的医疗器械,难以运用以往的分类经验来判断产品风险的高低。因此要对其进行严格的分类比较困难。目前,CFDA将定制增材制造(3D打印)骨科植入物等8类产品收录到《需进行临床试验审批的第三类医疗器械目录》中。
第二,就企业而言,3D打印设备与使用的材料是关系到产品质量的两大因素。随着3D打印设备的进步,打印材料也从无生物相容性的材料拓展到了活性细胞、蛋白及其他细胞外基质。对于不同的打印材料,质量控制有不同的关注点。
第三,就监管部门而言,采用3D打印技术制备的标准化医疗器械,制造工艺和材料的安全有效性是技术审评的重点。3D打印医疗器械的技术审评应该在审评方法、程序、重点关键点上与传统医疗器械不同,但目前还没有相关的规定出台。
由此可见,由于对逐层加工这种崭新的制造技术研究尚浅,对该技术制备医疗器械的全生命周期缺乏深入探索,对终产品的有效检测检验手段尚不明晰,对产品制造过程的验证、确认过程以及放行方式尚处于探索阶段,相关企业及其监管部门对3D打印医疗器械的技术评价还有一段较长的路要走,也会影响产品的上市审批进展。


0 留言