美国哈佛大学Kevin Kit Parker教授团队在《Nature Materials》期刊发表论文“Fibre-infused gel
scaffolds guide cardiomyocyte alignment in 3D-printed
ventricles”,开发了一种含有预制明胶纤维的水凝胶墨水,用于打印3D器官级支架,再现心脏的细胞内和细胞间组织。作者通过将预制明胶纤维添加到水凝胶中可以控制墨水流变性,实现受控的溶胶-凝胶转变,以实现独立3D结构的精确打印,而无需额外的支撑材料。在墨水挤压过程中,剪切诱导的纤维排列提供了微尺度的几何线索,促进了体外培养的人类心肌细胞向各向异性肌肉组织的自组织,3D打印心室体外模型具有仿生各向异性电生理和收缩特性。

WHAT——什么是明胶纤维?
明胶纤维是一种合成纤维,通常由明胶为原料制成,可以与天然的胶原纤维相媲美,其尺寸通常在1.3 μm到8.7
μm之间,这种纤维具有较好的力学性能,并且与某些细胞具有良好的相容性。明胶纤维与纤维表面的相互作用原理包括物理和化学相互作用,能增加纤维之间的接触面积,提高结合的强度。
WHY——为什么要用生物3D打印的方法来制造心脏组织?
目前研究人员更多是通过微接触印刷、光刻、定向冷冻干燥、纤维纺丝和微生理芯片制造来设计心脏组织,但这些方法在制造完全复制心脏功能的复杂几何组织的能力方面受到限制。而生物3D打印的优势就在于能够制造复杂、生物相容性更强的结构,可以精确地复制细胞和组织的原始结构。
HOW——作者通过将明胶纤维注入明胶和海藻酸盐(Gel-Alg)水凝胶基质来设计墨水。
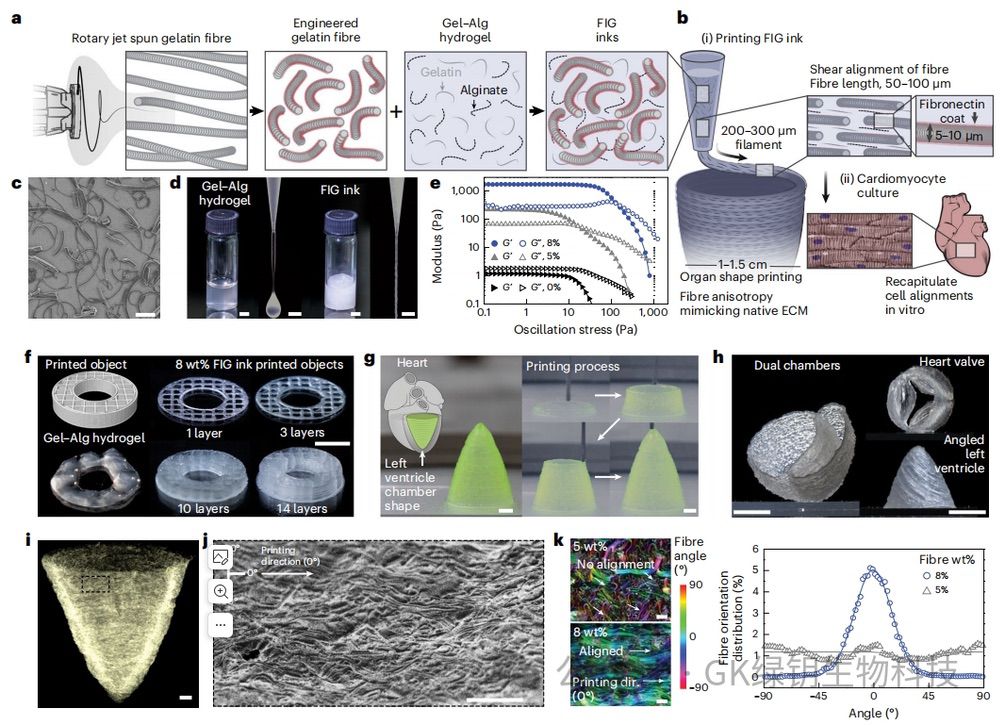
将纤维融入水凝胶中可以改变墨水的流变性,从而无需任何支撑结构或材料即可创建精确且复杂的3D支架。通过排列明胶微纤维的形式,结合拓扑和化学线索来打印的3D心室支架能促进心肌细胞自组织成各向异性肌肉组织。在制造纤维注入凝胶(FIG)墨水后,作者打印了由明胶纤维和Gel-Alg水凝胶组成的3D支架。在打印过程中,喷嘴内的剪切应力足以使具有弹性的FIG墨水变成液体,挤压后恢复其弹性稳定性。这些非线性流变特性允许FIG墨水连续挤压,还能够打印复杂的几何形状的分层结构,且无需牺牲层或牺牲浴作为支撑结构,实现自我支撑的空心3D结构。总之,凝胶状FIG墨水的高弹性模量提供了足够的凝胶稳定性,可以打印厚度在200
μm到350 μm之间的自支撑壁,而不需要支架或牺牲浴。
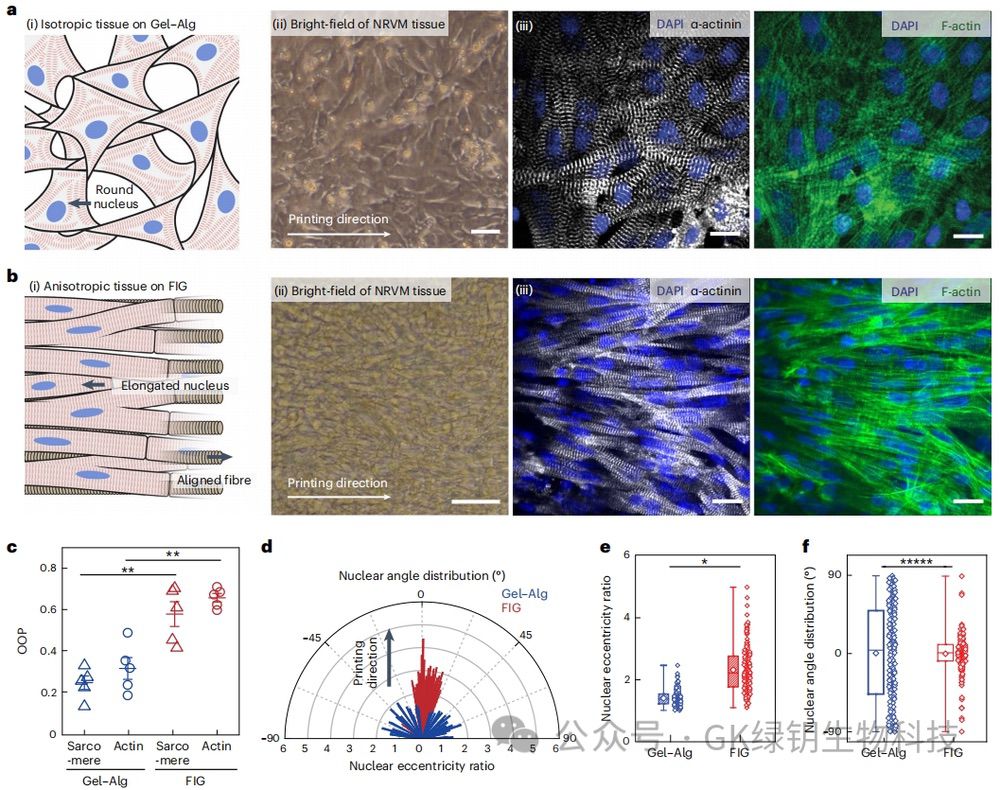
为了评估FIG墨水打印支架在增强心肌细胞的细胞内和细胞间组织、肌原纤维组织和排列的能力,作者将新生大鼠心室心肌细胞(NRVM)接种在打印的二维(2D)FIG支架上。结果得到高度排列的心脏组织的形成,相对于多形性培养条件保留了相当的细胞活力。接下来作者通过计算取向顺序参数(OOP)来测量结构组织的各向异性程度,该参数量化了肌聚体
α-肌动蛋白和细胞骨架肌动蛋白丝(F
-肌动蛋白)排列。细胞内和细胞间骨架结构产生的预应力决定了细胞核的伸长和取向,与对照Gel-Alg支架上的细胞核相比,FIG支架上的细胞核被拉长,NRVM的核取向也沿打印方向排列(0°),而Gel-Alg支架的核取向无特异性取向。
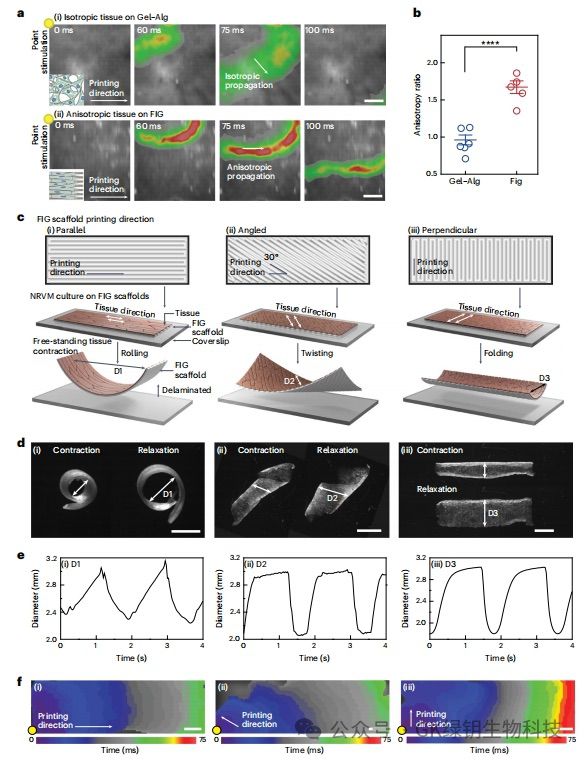
为了测试FIGs诱导心肌细胞沿纤维结构自组织并形成心脏功能合胞体的能力,作者测量细胞-细胞连接结构的功能后果及其电生理特性。作者使用光学作图来测量钙(Ca2+)瞬态传播,作为相对于打印方向沿纵向和横向轴的心脏脉冲传导的指标。最后结果表明,FIG支架上的心脏组织在6厘米的蛇形图案上传播Ca2+波,显示出沿打印方向的强大电耦合。利用NRVM和人诱导多能干细胞源性心肌细胞(hiPSC-CMs)在FIG支架上构建心脏组织的横纵传播速度值分别为1.67±0.085和1.62±0.18。相比之下,没有纤维的对照支架上的NRVM组织的传播速度比接近1。心肌细胞沿打印方向的优先机电耦合使其在电刺激下产生循环变形,在一个支架中交替排列方向也表明心肌细胞组织遵循局部纤维方向,导致相应的局部组织收缩模式。
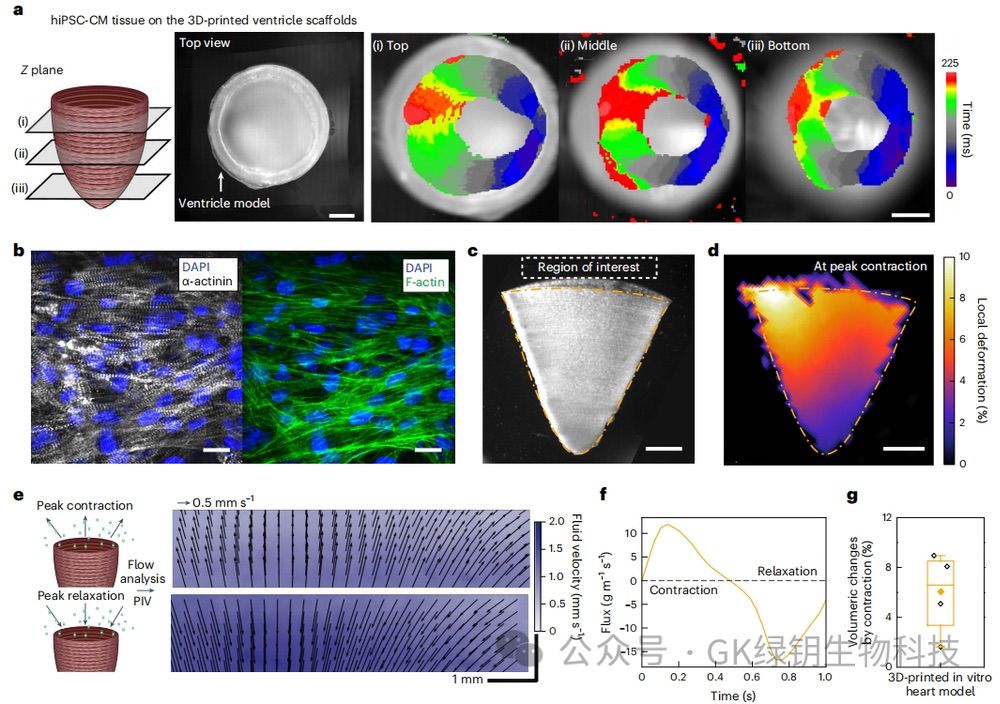
作者在3D打印的心室支架上培养NRVM和hiPSC-CMs,纤维呈圆周排列,形成三维心室形状的层状各向异性心脏组织。体外心室模型在培养中保持14天,自发心跳率为每秒~0.71次。这表明该支架在超过80万次的机械载荷循环中是耐用的,没有明显的退化。作者在对NRVM培养的脑室模型进行点电刺激后,观察到Ca2+在横向(打印方向)的瞬时传播速度比纵向更快。这证实了3D打印脑室支架中的脉冲传播也沿着组织排列发生,这是由打印方向决定的。为了评估hiPSC-CM心室模型的收缩性能,作者使用粒子成像测速
(PIV) 测量了基底开口处的流体动力学输出,粒子流的方向和速度使能够估计收缩和松弛期间流体运动的质量通量。最后计算出hiPSC-CM
培养心室模型的心室容积在峰值收缩和峰值舒张之间的变化为5.94±1.66%,比先前报道的NRVM和hiPSC-CM体外心室模型的数值(射血分数)分别高出2-5倍和8-20倍。
结论:作者展示了用基于水凝胶的FIG墨水3D打印组织工程心室模型的能力,该模型同时再现了心脏的微结构ECM结构和宏观结构器官水平几何形状。注入明胶纤维在水凝胶墨水中充当流变改性剂,能够在不使用牺牲浴的情况下打印复杂的3D物体。这些纤维还提供生化和微观结构线索,促进细胞粘附和自组织成为功能性合胞体。这项工作表明FIG墨水打印将在促进标准化和可访问的生物打印过程中发挥重要作用,以微结构精度再现天然器官几何形状。
原文链接:https://doi.org/10.1038/s41563-023-01611-3


0 留言