加州大学河滨分校和罗文大学的研究人员开发出一种能够自主供氧的生物工程补丁,解决了组织工程领域一个长期悬而未决的难题。这项研究也得到了加州大学伯克利分校、德克萨斯州塔勒顿州立大学以及洛杉矶特雷西生物医学创新研究所的贡献。该成果发表在《通讯-材料》期刊上,研究团队将这一平台称为智能自供氧组织系统(SSOT)。其工作原理是通过向一种特殊设计的凝胶施加微小电流,该凝胶含有水,通过电解作用将水分子分解为氧气和氢气。氧气可根据需求直接释放到周围组织中,而无需依赖血液供应。
这一点至关重要,因为细胞只有在距离血管约100至200微米(大约相当于两根人类头发的宽度)的范围内才能存活。在薄层组织样本中,氧气可以自然扩散。但要构建出具有临床实用厚度、未来有望替代受损器官或修复大面积伤口的组织,就意味着内部细胞距离任何血管都太远而无法存活。迄今为止尝试的所有方法,包括携氧分子、多孔支架以及刺激新血管形成的生长因子,都未能在新血管系统建立之前的关键窗口期内可靠地维持细胞存活。
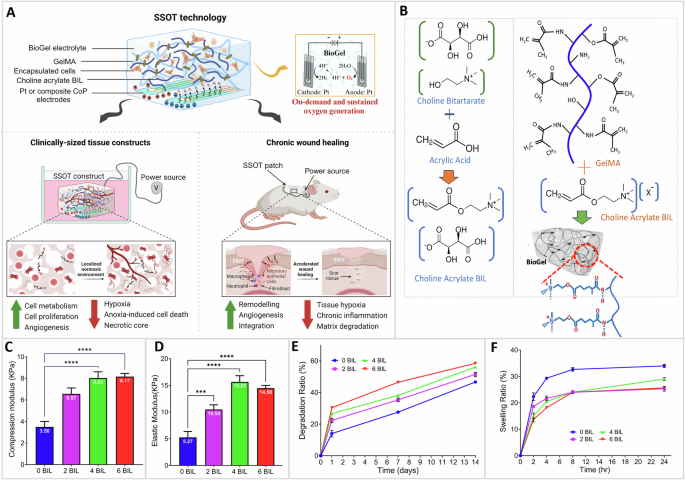
SSOT技术的特性及其在组织工程中的作用。图片来源:Vaishali Krishnadoss等人,《通信材料》。
从内部“工程化”供氧
SSOT系统通过直接在支架内部产生氧气来规避这一问题。该凝胶结合了甲基丙烯酰化明胶(GelMA)和一种由胆碱(一种人体自然产生的营养素)制成的生物离子液体。它们共同形成了一种具有导电性和粘附性的水凝胶,研究团队称之为BioGel,它既是传导电流的电解质,也是细胞生存和生长的环境。如研究所述,驱动反应的电极有两种版本。一种使用铂,这是此类电化学工作中可靠且经过充分研究的材料。另一种使用由磷酸钴、一种名为Laponite的粘土状矿物以及GelMA制成的复合电极,这种配方使其能够通过挤出式生物3D打印机打印成定制形状。这种可打印性最终可能让临床医生能够根据患者伤口或植入部位的具体轮廓定制电极几何形状。
源自胆碱的生物离子液体的贡献不止于导电性。以4%的浓度添加后,与纯GelMA相比,凝胶的硬度增加了一倍以上,并且显著减缓了酶促降解。在相同条件下,纯GelMA在三天内因胶原蛋白消化酶的作用损失了超过90%的质量,而BioGel配方在整整一周内仅损失了约25%。分子模拟有助于解释为何生物离子液体还能改善氧气输送:胆碱分子降低了氧气在铂表面的吸附强度,从而将更多氧气推向组织。
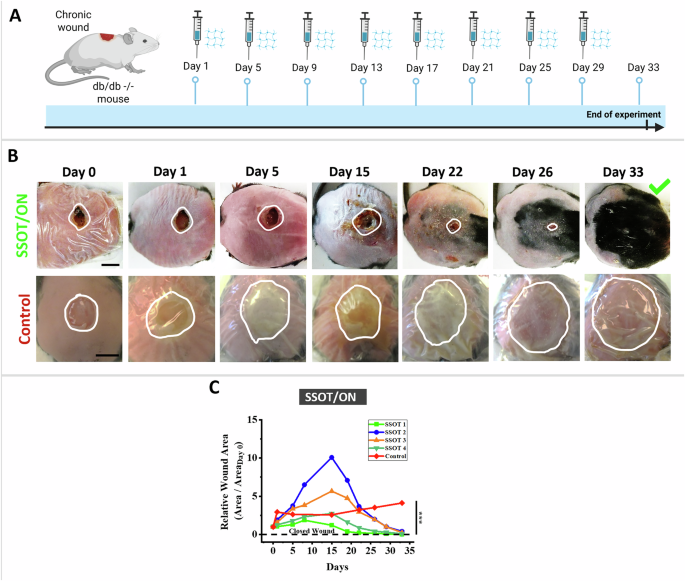
SSOT技术对糖尿病小鼠模型中慢性伤口愈合的影响。图片来源:Vaishali Krishnadoss等人,《通信材料》。
平台测试验证
在实验室细胞培养测试中,研究团队将三种不同的人类细胞类型嵌入SSOT构建体中,并使其暴露于严重的缺氧环境,大致相当于厚组织植入物深处的条件。两周后,SSOT组中的细胞存活率根据细胞类型不同,在74%到79%之间。在没有供氧系统的情况下,存活率降至38%到46%。该平台还增加了一种名为血管内皮生长因子(VEGF)的蛋白质的分泌,人体利用这种蛋白质来发出新血管生长的信号。
随后,研究人员将SSOT构建体植入大鼠皮下,以评估机体对装置的反应。28天后,免疫反应极小,巨噬细胞(通常标志着异物排斥的细胞)的浸润水平很低。这一结果对于任何旨在长期植入的设备都至关重要。然而,最具启示性的测试来自动物伤口愈合试验。研究团队在糖尿病小鼠身上测试了SSOT补丁,这些小鼠通过在受伤时抑制两种关键的抗氧化酶,被设计成会发展为慢性不愈合伤口,从而让皮肤上天然存在的细菌建立持续性感染。
这些伤口无法自行愈合,并且在未经治疗的动物中,在整个观察期内持续恶化。使用电池供电的SSOT补片治疗的小鼠在33天内显示出显著的伤口闭合,组织分析证实了有序的胶原蛋白形成和适当的皮肤层再生,而非瘢痕组织。该平台能否跨越人体临床试验的重大障碍尚待观察。该系统仅以1伏特电压运行,并在30天的开关循环中保持了稳定的电化学性能,但在大型动物以及最终在人体中的测试还在前方。作为一个概念验证,它为困扰组织工程数十年的难题提供了一个技术上可信的解决方案。
这项题为“用于生物工程组织构建体中局部和持续氧气输送的智能自供氧系统”的研究由Vaishali Krishnadoss、Baishali Kanjilal、Aihik Banerjee、Prince David Okoro、Mohammad Khavani、Proma Basu、Nourouddin Sharifi、Johnson V. John、Manuela Martins-Green、Amos Mugweru、Mohammad R. K. Mofrad、Arameh Masoumi和Iman Noshadi共同完成。
中国3D打印网编译文章!



0 留言